IPSC诱导分化的全脑类器官(Induced Pluripotent Stem Cell-Derived Whole Brain Organoids, iPSC-WBOs)是一种利用诱导多能干细胞(iPSCs)通过定向分化和自组织形成的,旨在模拟人脑整体结构和功能的三维(3D)细胞模型。这类模型旨在重现大脑不同区域的细胞组成、神经网络连接、功能区域划分以及部分高级认知功能。以下是对IPSC诱导分化的全脑类器官的详细介绍:1. iPSC来源与维持:
•细胞重编程:成体细胞(如皮肤成纤维细胞、血液细胞等)通过导入特定转录因子(如Oct4、Sox2、Klf4和c-Myc或其改良版本)转化为iPSCs,具有与胚胎干细胞相似的多能性。
•iPSC培养与扩增:维持iPSCs在特定培养条件下未分化状态,保持其多能性并进行扩增。
2. 神经祖细胞诱导与分化:
•神经前体细胞生成:通过调控培养基中的生长因子、小分子化合物等,引导iPSCs定向分化为神经祖细胞(neural progenitor cells, NPCs)。
•区域特异性分化:进一步调整培养条件,利用时空诱导策略(如梯度添加分化因子、立体培养、生物力学刺激等),促使NPCs分化为模拟不同脑区(如前脑、中脑、后脑、小脑等)特性的神经元和胶质细胞。
特性与应用:
结构与功能模拟:
•多脑区组成:iPSC-WBOs包含模拟不同脑区特性的神经元(如兴奋性神经元、抑制性神经元)、星形胶质细胞、少突胶质细胞等,形成类似大脑皮层、海马、丘脑等区域的结构特征。
•神经网络形成:类器官内部神经元之间形成突触连接,形成初级和次级神经回路,甚至展现出跨脑区的长距离投射。•电生理活动:分化出的神经元具有自发或诱发的电生理活动,可记录到动作电位、局部场电位等电信号,部分模型还能表现出自发或刺激诱发的网络级同步活动。
疾病建模:
•遗传性疾病:通过引入患者特异性的遗传突变,iPSC-WBOs可用于模拟神经发育障碍(如自闭症、精神分裂症、癫痫等)、神经退行性疾病(如阿尔茨海默病、帕金森病等)等,研究疾病发病机制、筛选治疗药物。•复杂疾病模型:结合CRISPR/Cas9等基因编辑技术,构建携带复合突变或表观遗传修饰的类器官,研究复杂神经疾病的病理过程。
药物筛选与毒性测试:
•高通量筛选:利用iPSC-WBOs平台进行药物筛选,评估候选药物对神经细胞功能、神经网络、信号通路的影响,预测药物疗效与神经毒性。
•个性化药物筛选:基于患者特异性的iPSC-WBOs,可进行个体化药物敏感性测试,为精准神经精神疾病治疗提供依据。
.基础神经科学研究:
•神经发育与演化:研究早期神经系统的形成、神经元迁移、神经网络构建等过程,揭示大脑发育的分子机制和调控因素。
•高级认知功能探索:尽管目前全脑类器官尚不能完全模拟人脑的复杂功能,但随着技术进步,部分模型已展现出简单的学习、记忆、感知等功能,为研究高级认知功能的细胞和网络基础提供平台。
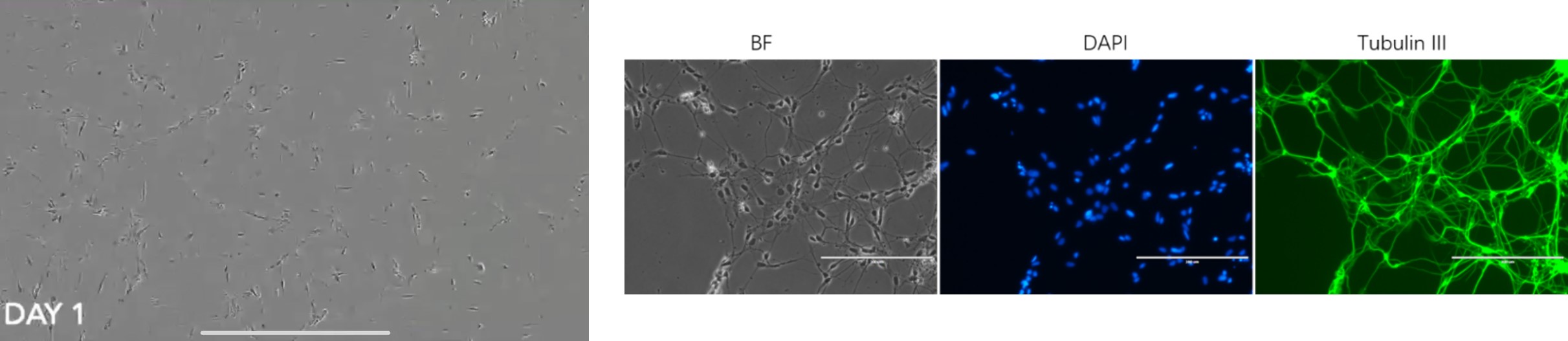
体外定向分化神经元和网络化
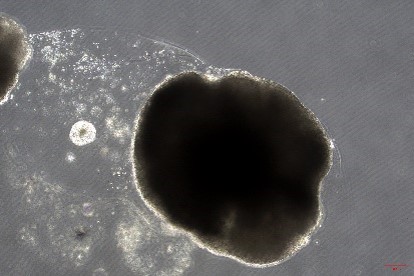
体外构建脑类器官
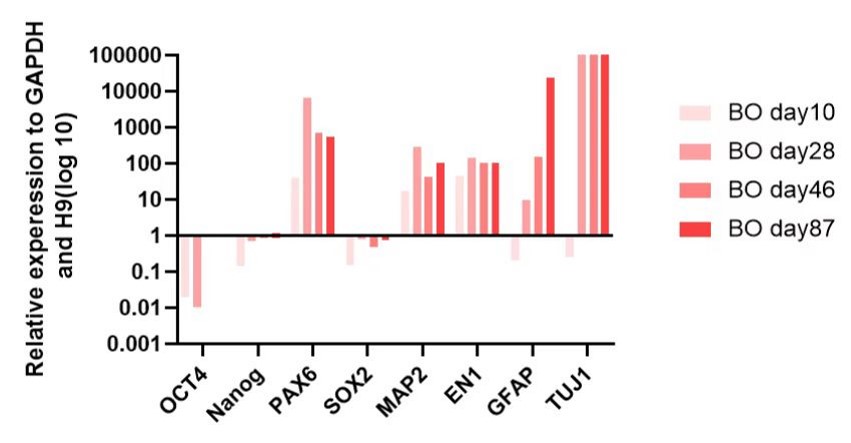
脑类器官中特异性基因表达上升
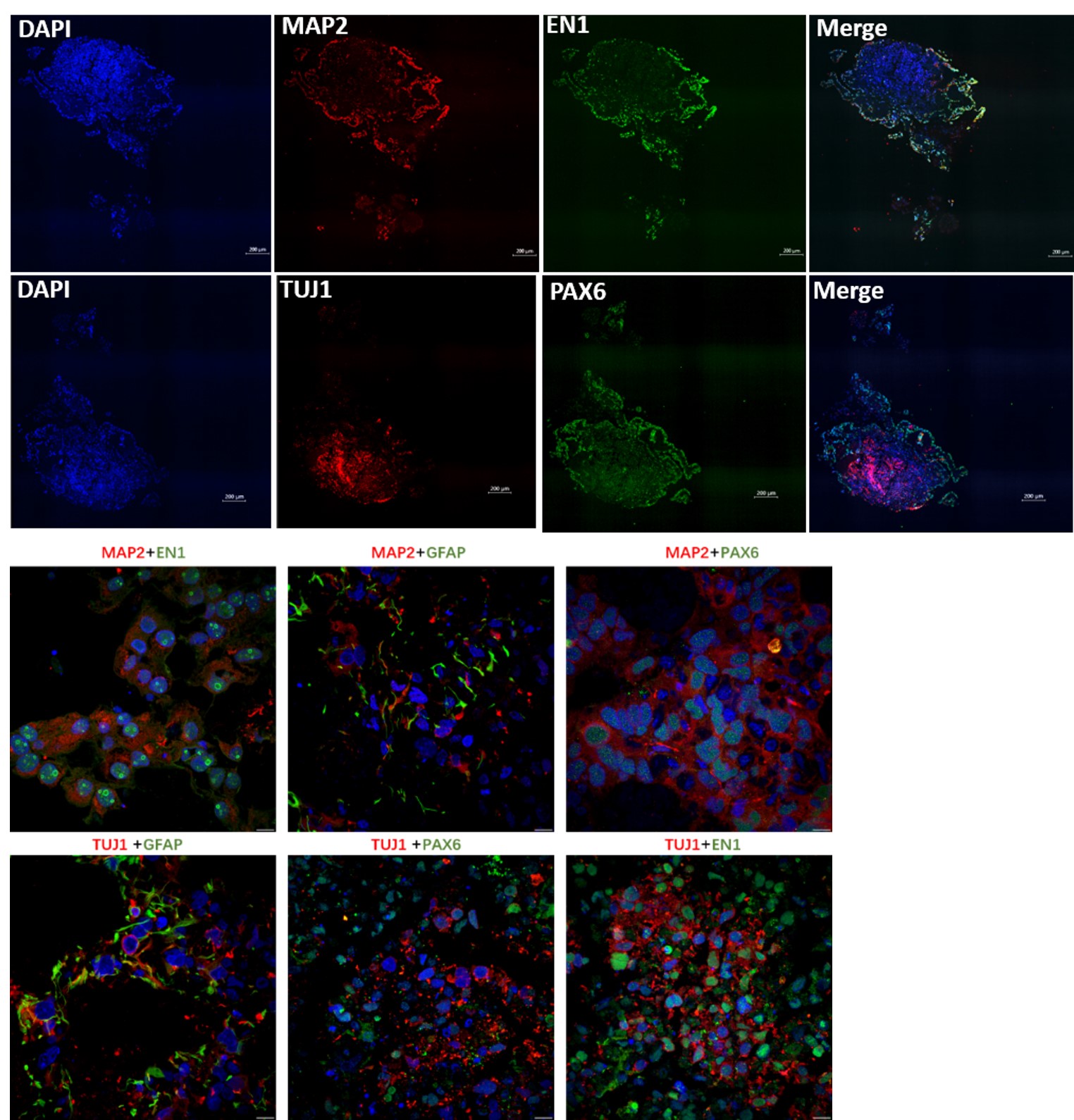
脑类器官的免疫荧光鉴定